A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.D与A同周期,其最高正价与最低负价代数和为零.A、E可形成AE3型分子,分子中只存在极性键.
(1)B元素在元素周期表中的位置是______.
(2)C的离子结构示意图为______,用电子式表示AE3的形成过程:______.
(3)由元素A、C及氢元素形成的化合物中含有的化学键的类型有______.
(4)请设计一个实验来说明D与A的非金属性强弱(写出化学方程式即可)______.
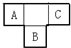
设A的质子数为x,则B的质子数为x+9,C的质子数为x+2,则有x+x+2=x+9,x=7,则A为N元素,B为S元素,C为F元素,D与A同周期,其最高正价与最低负价代数和为零,则D为C元素,A、E可形成AE3型分子,分子中只存在极性键,应为NH3,则E为H元素,
(1)B为S元素,原子序数为16,原子核外有3个电子层,最外层电子数为6,则应位于第三周期VIA族,故答案为:第三周期VIA族;
(2)C为F元素,原子核内有9个质子,对应的离子核外有8个电子,2个电子层,则离子的结构示意图为
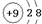
,NH3为共价化合物,用电子式表示的形成过程为
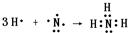
,故答案为:
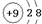
;
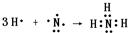
;
(3)由元素A、C及氢元素形成的化合物为NH4F,为离子化合物,含有离子键和极性共价键,故答案为:离子键、极性共价键;
(4)A为N元素,D为C元素,N的非金属性较C强,所对应的最高价氧化物的水化物的酸性也强,将硝酸加入到碳酸钠溶液中可发生反应:2HNO3+Na2CO3=2NaNO3+H2O+CO2↑,可用以证明C与N的非金属性强弱,
故答案为:2HNO3+Na2CO3=2NaNO3+H2O+CO2↑(或其他合理方法).
