W、X、Y和Z都是周期表中前18号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为W2Y离子化合物;
②Y和Z属同族元素,它们能形成两种气态化合物;
③X和Y属同一周期元素,它们能形成组成为XY2共价化合物,一个XY2分子中的电子总数为22;
(1)W元素是______;Z元素是______.
(2)化合物W2Y和XY2的电子式分别是______和______.
(3)Y和Z形成的两种气态化合物的分子式是______和______.
(4)写出化合物XY2与W的高价氧化物对应水化物反应的离子方程式:______.
W、X、Y和Z都是周期表中前18号元素,Y和Z属同族元素,它们能形成两种气态化合物,化合物为SO2、SO3,则Y、Z可能为O或S;若Y为O,由X和Y属同一周期元素,它们能形成组成为XY2共价化合物,一个XY2分子中的电子总数为22,X的质子数为22-8×2=6,则X为C;若Y为S,则X的质子数为22-16×2=-10,不符合事实,则Y为O,Z为S,X为C;W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为W2Y离子化合物,则W为Na,
(1)W为Na,Z为S,故答案为:Na;S;
(2)化合物W2Y为Na2O,为离子化合物,电子式为
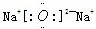
,XY2为CO2,为共价化合物,电子式为
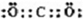
,
故答案为:
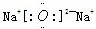
;
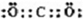
;
(3)Y为O,Z为S,形成两种气态化合物为SO2、SO3,故答案为:SO2;SO3;
(4)W的高价氧化物对应水化物为NaOH,与CO2反应生成碳酸钠和水,离子反应为CO2+2OH-═CO32--+H2O,故答案为:CO2+2OH-═CO32--+H2O.
