问题
问答题
某金属元素R的单质0.9g与硫酸完全反应时可生成R2(SO4)3,并生成1.12L氢气(标准状况).已知该元素的原子核中有14个中子.试通过计算确定该元素的名称及其在周期表中位置.
答案
令0.9g金属的物质的量为n,根据电子转移守恒,则:
n×3=
×2,解得n=1.12L 22.4L/mol
mol,1 30
所以金属R的摩尔质量为M=
=27g/mol,0.9g
mol1 30
所以R元素的相对原子质量为27,
R元素原子的质子数为Z=A-N=27-14=13,
故该元素为铝,原子结构示意图为
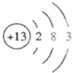
,位于第三周期第ⅢA族.
答:该元素的名称为铝,位于元素周期表中第三周期第ⅢA族.
