(6分)根据图示情景和范例,编写计算题,并完成相关内容。
【情景1】要配制一定质量分数、一定质量的氯化钾溶液,应该怎么操作?
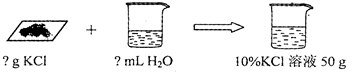
(1)编题范例 配制10%的氯化钾溶液50g,分别需氯化钾固体和水各多少?
(2)配制该溶液的操作步骤
①计算: ▲
②称量:用托盘天平称取所需固体,再用 ▲ mL的量筒量取所需的水;
③溶解:将称得的氯化钾固体放入烧杯中,再倒入量取的水,用玻璃棒充分搅拌;
④装瓶:将配制的溶液倒入试剂瓶,并贴上标签。
【情景2】已知一定质量分数、一定质量的氢氧化钾溶液与一定质量的盐酸反应,得到只有一种溶质的溶液,求算反应后溶液的溶质质量分数。
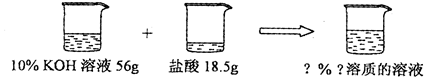
(1)编写题目 ▲
(2)计算过程 ▲

分析:〔情景1〕(2)①溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量,体积=质量÷密度;
②量筒的选用,容量需大于称量的溶液体积;
〔情景2〕(1)编写的题目要结合情景中的图示内容和数据;
(2)利用氢氧化钾与盐酸反应的化学方程式和氢氧化钾的质量,列出比例式,就可计算出生成氯化钾的质量(即溶质质量),然后根据溶质质量分数公式计算即可.
解答:解:〔情景1〕(2)①需氯化钾固体的质量为:50g×10%=5g;
需水的质量为:50g-5g=45g,
水的体积为:45g÷1g/mL=45mL;
②因为所需水的体积为45mL,故需用容量为50mL的量筒量取所需的水;故答案为:50;
〔情景2〕(1)56g10%的氢氧化钾溶液与18.5g某浓度的盐酸恰好完全反应,计算反应所得溶液中溶质的质量分数.
(2)解:设完全反应后,生成氯化钾的质量为x,
KOH+HCl=KCl+H2O
56 74.5
56g×10%,x
∴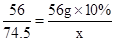 ,
,
解之得:x=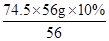 =7.45g;
=7.45g;
反应所得溶液中溶质的质量分数为: ×100%=10%.
×100%=10%.
答:反应所得溶液中溶质的质量分数为10%.
