已知:J、L、M、R、T是原子序数依次增大的短周期主族元素;J元素最低负化合价的绝对值与其原子最外层电子数相等;L的最简单气态氢化物甲的水溶液显碱性;M是地壳中含量最多的金属元素;R形成简单的阴离子R2-与Ar的电子层结构相同.则
(1)M的离子电子式为______;
(2)元素T在周期表中的位置是______;
(3)用电子式表式JR2的形成过程______;
(4)M和T形成的化合物(MT3)在潮湿的空气中冒白色烟雾,反应的化学方程式为:______.(提示:此反应为非氧化还原反应).
(5)在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为______.
J元素最低负化合价的绝对值与其原子最外层电子数相等,说明J的最低化合价与最高化合价绝对值相等,则J最外层电子数为4,L的最简单气态氢化物甲的水溶液显碱性,则L为N元素,由原子序数关系可知J为C元素,R形成简单的阴离子R2-与Ar的电子层结构相同,则R应为S元素,M是地壳中含量最多的金属元素,应为Al元素,而T是原子序数最大的元素,且为短周期主族元素,应为Cl元素,
(1)M为Al,对应离子的电子式为Al3+,故答案为:Al3+;
(2)T为Cl元素,原子序数为17,原子核外有3个电子层,最外层电子数为7,位于周期表第三周期ⅦA族,
故答案为:第三周期ⅦA族;
(3)JR2为CS2,用电子式可表示形成过程为
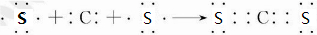
,
故答案为:
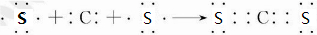
;
(4)AlCl3可发生水解,生成Al(OH)3和HCl,HCl易结合空气中水蒸气而形成白雾,方程式为AlCl3+3H2O⇌Al(OH)3+3HCl,
故答案为:AlCl3+3H2O⇌Al(OH)3+3HCl;
(5)甲为氨水溶液,与H2O2反应生成的产物不污染环境,则应生成N2和H2O,反应的化学方程式为2NH3•H2O+3H2O2═N2+8H2O,
故答案为:2NH3•H2O+3H2O2═N2+8H2O.
