(12分)已知由短周期元素组成的五种常见化合物分子A、B、C、D、E,其所含原子数目依次为2、3、4、5、6,其中A、B、E各含18个电子,C、D各含10个电子。请回答:
(1)D中含有的化学键类型有 ,若实验测得在25℃、101kPa时,8gD与O2完全燃烧,生成稳定化合物时放出445kJ的热量,则该反应的热化学方程式为 。
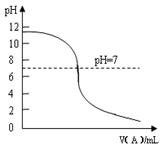
(2)室温下,向一定量C的稀溶液中逐滴加入A的稀溶液,有离子化合物XY4Z(X、Y、Z表示元素符号)生成,混合液pH变化如图所示。实验过程中,当pH=7时,下列关于混合液中离子浓度判断正确的是 。
Ⅰ. c(XY+4)>c(Z—)>c(OH—)=c(H+)
Ⅱ. c(XY+4)=c(Z—),c(OH—)=c(H+)
Ⅲ. c(Z—)>c(XY+4)> c(OH—)=c(H+)
Ⅳ. c(XY+4) + c(H+) = c(Z—) + c(OH—)
(3)XY4Z溶液PH 7(填“小于、等于、大于”),其原因用离子方程式表示为: 。
(4)将B缓慢通入Cu(OH)2悬浊液中,浑浊变为黑色,原因是 。
(5)E的核磁共振氢谱图中有两组峰,且峰覆盖的面积比为3︰1 ,E的结构式为: 。
(12分)
(1)共价键(1分)
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=—890kJ·mol—1(2分)
(2)Ⅱ、Ⅳ(2分)
(3)小于(1分)NH+4 + H2O  NH3·H2O + H+ (2分)
NH3·H2O + H+ (2分)
(4)CuS的溶解度小于Cu(OH)2的溶解度(2分)
(5)CH3-OH(2分)
