已知:①红磷在氯气中燃烧可以生成两种化合物——PCl3和PCl5,氮与氢也可形成两种化合物——NH3和NH5。
②PCl5分子中,P原子的1个3s轨道、3个3p轨道和1个3d轨道发生杂化形成5个sp3d杂化轨道,PCl5分子呈三角双锥形(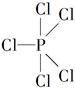 )。
)。
(1)NH3、PCl3和PCl5分子中,所有原子的最外层电子数都是8个的是________(填分子式),该分子空间构型是______________。
(2)有同学认为,NH5与PCl5类似,N原子的1个2s轨道、3个2p轨道和1个2d轨道可能发生sp3d杂化。请你对该同学的观点进行评价__________________________
(3)经测定,NH5中存在离子键,N原子最外层电子数是8,所有氢原子的最外层电子数都是2,则NH5的电子式是________。
(4)肼(N2H4)分子可视为NH3分子中的一个氢原子被——NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子空间构型为 ,N2H4分子中氮原子轨道的杂化类型是 。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g);△H=-1 038.7 kJ·mol-1
若该反应中有4 mol N-H键断裂,则形成的π键有 mol。
③肼能与硫酸反应生成N2H6SO4,N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在 (填标号)。
a.离子键 b.共价键
c.配位键 d.范德华力
(1)PCl3 三角锥形 (2)不对,因为N原子没有2d轨道
(3)  (4)三角锥形 sp3杂化 3 d
(4)三角锥形 sp3杂化 3 d
题目分析:(1)H只有2电子,PCl5分子中的P有10电子;(4)①NH3分子空间构型为三角锥形,N原子为sp3杂化,根据题干中给出的信息可知N2H4分子中氮原子轨道的杂化类型也是sp3。
②反应中有4 mol N-H键断裂,即有1 mol N2H4反应,根据反应方程式可知,1 mol N2H4参加反应有1.5 mol N2生成,而每摩尔N2中有2 mol π键。
③该题为信息题,知道(NH4)2SO4分子中存在的化学键(离子键、共价键、配位键)即可解答。
点评:物质的结构是高考历年的重点,考生在备考中要注意区分各概念,熟练运用概念进行相关的判断。
