2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致
发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8一羟基喹啉铝等。
(1)Mn2+在基态时,核外电子排布式为_________。
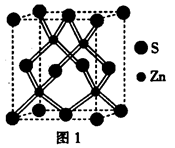
(2)硫化锌的晶胞结构如图1所示,则每个晶胞中含S2-的数目为________个。
(3)蒽(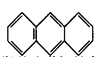 ,平面结构)属于________(填“极性”或“非极性”)分子。
,平面结构)属于________(填“极性”或“非极性”)分子。
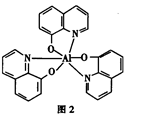
(4)8一羟基喹啉铝具有较高的发光效率。8一羟基喹啉铝的分子结构如图2所示,其分子中存在的相互作用力有_______(填字母)。
A.极性键 B.非极性键 C.金属键 D.氢键 E.配位键
(5)已知铜元素能形成多种化合物。
①CuSO4·5H2O也可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图3所示。下列说法正确的是________(填字母)。
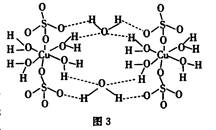
A.在上述结构示意图中,所有氧原子都采用SP3杂化
B.该晶体中电负性最大的元素是O
C.该晶体属于原子晶体
D.该晶体中的水在不同温度下会分步失去
②YBCO-12也是一种含Cu元素的化合物,化学式为YBa2Cu3O6.95。已知该化合物中各元素的化合价为:Y为+3价、Ba为+2价、O为—2价、Cu为+2价和+3价。则该化合物中+2价Cu和+3价Cu的原子个数之比为_______。
(8分)
(1)1s22s22p63s23p63d5(或[Ar] 3d5)(2分)
(2)4(1分)
(3)非极性(1分)
(4)ABE (2分)
(5)①BD(2分)②7:3(1分)
题目分析:
(1)Mn2+在基态时,核外电子排布式为1s22s22p63s23p63d5。
(2)硫化锌的晶胞结构如图1所示,则每个晶胞中8个顶点各有1/8,6个面各有1/2,共4个。
(3)分子是平面型,有高度的对称性,属于非极性分子。
(4)C-C的非极性键,C-O、C-N的极性键,N-Al的配位键(共用N的一对孤对电子)。
(5)①A.H2O中氧原子都采用SP3杂化,硫酸根中不是,错误;B.该晶体中电负性最大的元素是O,正确;C.该晶体属于离子晶体,错误;D.该晶体中的水是用不同的键结合的,所以在不同温度下会分步失去,正确。②根据化合价代数和为0,求得Cu平均价态为2.3价,进一步求得+2、+3价原子数目比为7:3
