下表是元素周期表的一部分,其中A—G分别代表一种元素。
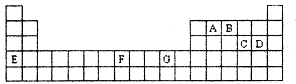
请根据表中所列元素,回答下列问题:
(1)所列元素中第一电离能最小的是 (填元素符号);D元素原子核外有 种不同运动状态的电子;基态原子的价电子层中,未成对电子数最多的元素是 (填元素符号)。
(2)AC2分子的空间构型是 ,该分子中A原子的杂化方式为 。
(3)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物的溶解度,原因是 。
(4)基态G2+的核外电子排布式是 ,乙二胺(结构简式为H2N—CH2一CH2—NH2)分子中的碳原子的杂化方式为 ,G2+与乙二胺可形成配离子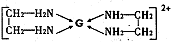 该配离子中含有的化学键类型有 (填字母编号)。
该配离子中含有的化学键类型有 (填字母编号)。
a.配位键 b.极性键 c.离子键 d.非极性键
(5)化合物EF[F(AB)6]是一种常见的蓝笆晶体,其中的AB—与B2为等电子体,则、AB—的电子式为 。下图为该蓝色晶体晶胞的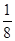 (E+未画出),该蓝色晶体的一个晶胞中E+的个数为 个。
(E+未画出),该蓝色晶体的一个晶胞中E+的个数为 个。
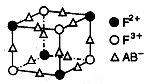
(1)K 17 Fe
(2)直线型 SP
(3)NH3与H2O分子之间存在氢键,CH4、H2S和H2O分子间不存在氢键
(4)1s22s22p63s23p63d9 SP3 abd
(5)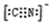 4
4
题目分析:
(1)根据题意,A是C,B是N,C是S,D是Cl,E是K,F是Fe,G是Cu。第一电离能最大的是K。D是17号元素氯,有17种不同运动状态的电子。Fe的未成对电子数为4。
(2)CS2的与CO2的结构相同,所以也是直线型,SP杂化类型。
(3)NH3与H2O分子之间存在氢键,CH4、H2S和H2O分子间不存在氢键
(4)Cu2+的核外电子排布式是1s22s22p63s23p63d9,乙二胺中的碳原子形成的是单键,所以其杂化方式为 SP3。配离子中的化学键有非极性键、极性键、Cu2+与N之间是配位键。
(5)据“AB—与B2为等电子体”,则CN-的电子数也为14。据图知,F2+为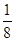 X4,F3+为
X4,F3+为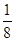 X4,AB-为
X4,AB-为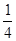 X12=3,根据电荷数整体为0的原则,该蓝色晶体晶胞的
X12=3,根据电荷数整体为0的原则,该蓝色晶体晶胞的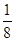 (E+未画出),
(E+未画出),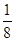 个中的E+为
个中的E+为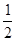 。则该蓝色晶体的一个晶胞中E+的个数为8x1/2="4"
。则该蓝色晶体的一个晶胞中E+的个数为8x1/2="4"
