化学中的某些元素是与生命活动密不可分的元素。请回答下列问题:
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式分别是________,NO3—的空间构型为____________。
(2)A、B、C三元素的原子序数依次增大,它们原子的最外层电子排布均为4s1。
①B元素基态原子电子排布式为___________________________________________。
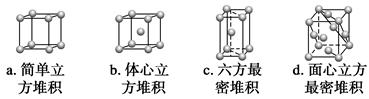
②A元素单质的晶体堆积模型为________(填字母),其空间利用率为__________。
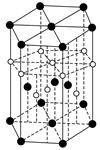
③氢元素与C元素可形成一种红色化合物,其晶体结构单元如下图。则该化合物的化学式为__________(小白球表示H,小黑球表示C)。
(3)已知氮化硼(BN)的一种晶体结构与金刚石相似,则B—N—B之间的夹角是________,氮化硼的密度为3.52 g·cm-3,则B—N键的键长是________pm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
(1)sp3、sp2杂化 平面三角形
(2)①1s22s22p63s23p63d54s1或[Ar]3d54s1
②b 68%
③CuH
(3)109°28′ 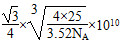
(1)NH4+为正四面体结构,所以N原子的杂化方式为sp3,NO3—中含有3对价层电子对,其离子构型为平面三角形,N原子采取sp2杂化。
(2)A、B、C的价电子构型分别为4s1、3d54s1、3d104s1,所以A为K,B为Cr,C为Cu。K为体心立方堆积,Cu为面心立方最密堆积,体心立方堆积的空间利用率为68%,而面心立方最密堆积的空间利用率为74%。
③H( )∶6×
)∶6×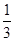 +1+3=6
+1+3=6
Cu( )∶12×
)∶12×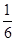 +2×
+2×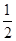 +3=6
+3=6
其化学式为CuH。
(3)BN的基本结构单元为正四面体,所以B—N—B之间的夹角为109°28′。一个金刚石晶胞中含有C原子数为8×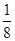 +6×
+6×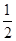 +4=8个,所以一个BN晶胞中含有4个B原子,4个N原子,设晶胞的棱长为a cm,则B—N的键长为
+4=8个,所以一个BN晶胞中含有4个B原子,4个N原子,设晶胞的棱长为a cm,则B—N的键长为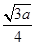 (为体对角线的
(为体对角线的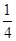 )。
)。
a3·3.52×NA=4×25
a=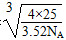
所以其键长为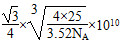 pm。
pm。
