原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为24。
(1)F原子基态的核外电子排布式为 。
(2)在A、B、C三种元素中,第一电离能由大到小的顺序是 (用元素符号回答)。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是 。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为 。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为 。
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为 。
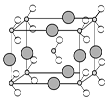
(1)[Ar]3d54s1(2分)
(2)N>O>C(2分)
(3)B的氢化物分子之间存在氢键(2分)
(4)[N=C=O]-(2分)
(5)sp(2分)
(6)NaNO2(2分)
题目分析:A、B、C、D、E、F分别为C、N、O、Na、S、Cr。(2)N原子最外层电子为半满的相对稳定结构,第一电离能较大,顺序为N>O>C;(3)氨气分子间存在氢键,溶沸点高;(4)该离子与二氧化碳等电子体,结构与二氧化碳相似,故为[N=C=O]-,注意带电荷;(5)该物质为二硫化碳,结构同二氧化碳,碳原子为sp杂化;(6)晶胞顶点上为原子团个数为8×1/8+1=2,棱上为钠离子,个数为8×1/4=2,故化学式为NaNO2。
