问题
填空题
一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4·H2O)是一种重要的染料及农药中间体。请回答下列相关问题:
(1)Cu的核外电子排布式为 。
(2)N的L层中有 对成对电子;N 立体构型是 ,其中心原子的杂化方式为 。
立体构型是 ,其中心原子的杂化方式为 。
(3)氨水溶液中存在多种氢键,任表示出其中两种 ;
(4)[Cu(NH3)4]SO4·H2O中呈深蓝色的离子是 ,该微粒中的“电子对给予一接受键”属于 键;
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式 。

答案
(1)1s22s22p63s23p63d104s1
(2)1 正四面体 sp3
(3)O—H…N N—H…O(或O—H…O)
(4)[Cu(NH3)4]2+ 配位(或共价)
(5)CuCl
(1)Cu在第4周期ⅠB族,电子排布为1s22s22p63s23p63d104s1;(2)N的电子排布式为1s22s22p3,L电子层即第二能层,因此只有1对成对电子,N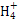 中心原子氮原子采用sp3杂化,空间构型为正四面体形;(3)氨水溶液中氨气分子和氨气分子之间可以形成氢键,水分子和水分子之间可以形成氢键,水分子和氨气分子之间也可以形成氢键(两种形式),氢键通常用“…”表示;(4)配离子[Cu(NH3)4]2+使溶液呈深蓝色,该离子中含有配位键;(5)均摊法,该晶胞中含有铜原子8×
中心原子氮原子采用sp3杂化,空间构型为正四面体形;(3)氨水溶液中氨气分子和氨气分子之间可以形成氢键,水分子和水分子之间可以形成氢键,水分子和氨气分子之间也可以形成氢键(两种形式),氢键通常用“…”表示;(4)配离子[Cu(NH3)4]2+使溶液呈深蓝色,该离子中含有配位键;(5)均摊法,该晶胞中含有铜原子8× +6×
+6× =4个,氯原子4个,两者是1∶1的关系,因此该氯化物的化学式为CuCl。
=4个,氯原子4个,两者是1∶1的关系,因此该氯化物的化学式为CuCl。
