VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为 。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为 。
(3)NH3的沸点比PH3高,原因是 ;PO43-离子的立体构型为 。
(4)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为 。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因 。
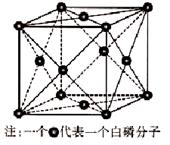
(6)磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如下图。已知最近两个白磷分子间的距离为 a pm,阿伏加德罗常数的值为NA,则该晶体的密度为 g/cm3(只要求列算式,不必计算)。
(1)1s22s22p63s23p63d104s24p3
(2)N>P>As
(3)NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力(合理答案均计分) 正四面体
(4)sp3杂化
(5)H3AsO4和H3AsO3可表示为(HO)3AsO和(HO)3As,H3AsO3中的As为+3价,而H3AsO4中的As为+5价,正电性更高,导致As-O-H中O的电子更向As偏移,更易电离出H+(合理答案均计分)
(6)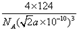 或
或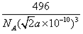 (3分,其他合理答案也计分)
(3分,其他合理答案也计分)
题目分析:(1)砷是33号元素,根据构造原理得基态原子的电子排布式为1s22s22p63s23p63d104s24p3
(2)同主族元素从上到下第一电离能逐渐减小,所以N、P、As原子的第一电离能由大到小的顺序为N>P>As
(3)NH3的沸点比PH3高,是因为NH3分子间存在较强的氢键,而PH3分子间仅有较弱的分子间作用力;根据分子立体构型的计算方法,PO43-离子的价层电子对是4,无孤对电子,所以立体构型为正四面体
(4)AsH3中As的价层电子对数是4,所以杂化轨道数也为4,因此杂化轨道类型是sp3杂化
(5)对于同种元素的含氧酸来说,该元素的化合价越高,其含氧酸的酸性越强。H3AsO4和H3AsO3可表示为(HO)3AsO和(HO)3As,H3AsO3中的As为+3价,而H3AsO4中的As为+5价,正电性更高,导致As-O-H中O的电子更向As偏移,越易电离出H+,酸性越强;
(6)在该晶胞中,实际含有4个白磷分子,其质量为4×31×4/NAg,最近两个白磷分子间的距离为 a pm,则立方体的棱长是√-2-apm=√-2-a×10-10m,所以该晶体的密度ρ=m/V=496/[NA (√-2-a×10-10)3]。
