氯化硼(BN)晶体是一种新型无机合成材料。用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2B4O7+ 2CO(NH2)2=4BN+Na2O +4H2O+2CO2↑,根据要求回答下列问题:
(1)组成反应物的所有元素中,第一电离能最大的是___________________。
(2)尿素分子(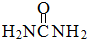 )中
)中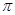 键与
键与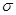 键数目之比为__________;尿素分子中处于同一平面的原子最多有_______个。
键数目之比为__________;尿素分子中处于同一平面的原子最多有_______个。
(3)尿素分子一定条件下形成六角形“超分子”(结构如图)。“超分子”中尿素分子间主要通过什么作用力结合。答:________________(填1种)。
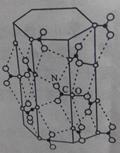
(4)图示“超分子”的纵轴方向有一“通道”。直链烷烃分子刚好能进人通道,并形成“超分子”的包台物;支链烷烃因含有测链,空间体积较大而无法进入“通道”。利用这一性质可以实现直链烷烃和支链烷烃的分离。
①直链烷烃分子能进人通道时,通过什么作用力与“超分子”结合,从而形成 “超分子”包合物?答:___________________。
②下列物质可以通过尿素“超分子”进行分离的是____________。
A.乙烷和丁烷 B.丁烷和异丁烷 C.异戊烷和新戊烷 D氯化钠和氯化钾
(5)BN晶体有a、B两种类型,且a—BN结构与石墨相似、B—BN结构与金刚石相似。
①a一BN晶体中N原子杂化方式是____________________;
②B—BN晶体中,每个硼原予形成________个共价键。这些共价键中,有________个为配位键。
(1)N(2分)
(2)1︰7(2分) 6(2分)
(3)氢键(2分)
(4)①范德华力(1分) ②B(1分)
(5)①sp2(1分) ②4 1(各1分,共2分)
题目分析:(1)组成反应物的所有元素Na、B、O、C、N、H,非金属性越强第一电离能越大。但由于氮元素的2p轨道电子处于半充满状态,稳定性强,所以氮元素的第一电离能大于氧元素的,即组成反应物的所有元素中,第一电离能最大的是N。
(2)单键都是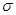 键,双键是由1个
键,双键是由1个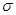 键和1个
键和1个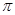 键构成的,所以根据尿素分子的结构简式
键构成的,所以根据尿素分子的结构简式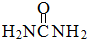 可知,分子中
可知,分子中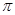 键与
键与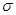 键数目之比为1︰7;由于碳氧双键是平面形结构,2个氮原子位于这个平面上。由于氨气是三角锥形结构,因此氨基中的2个氢原子最多有1个位于这个平面上,因此尿素分子中处于同一平面的原子最多有6个。
键数目之比为1︰7;由于碳氧双键是平面形结构,2个氮原子位于这个平面上。由于氨气是三角锥形结构,因此氨基中的2个氢原子最多有1个位于这个平面上,因此尿素分子中处于同一平面的原子最多有6个。
(3)尿素形成的晶体是分子晶体,而氧元素与氮元素均能形成氢键,所以“超分子”中尿素分子间主要通过氢键作用力结合。
(4)①烷烃形成的晶体类型是分子晶体,因此通过分子间作用力即范德华力与“超分子”结合,从而形成 “超分子”包合物。
②关节炎题意可知,可以实现直链烷烃和支链烷烃的分离,而乙烷和丁烷都不带支链,异戊烷和新戊烷均带支链,氯化钠和氯化钾不是烷烃,因此不能实现分离,丁烷和异丁烷分别是直链烷烃和支链烷烃,可以实现分离,答案选B。
(5)①a—BN结构与石墨相似,而石墨是层状结构,碳原子是sp2杂化,所以a一BN晶体中N原子杂化方式是sp2杂化。
②B—BN结构与金刚石相似,金刚石中每个碳原子形成4个共价键,所以B—BN晶体中,每个硼原予也形成4个共价键。由于B原子的最外层电子数是3个,只能形成3个共价键,因此这些共价键中,有1个为配位键。
