(14分)有A、B、C、D、F、G六种短周期主族元素,它们的原子序数依次增大。B元素的最高正价与最低负价的绝对值相等,D元素原子最外层电子数是次外层电子数的3倍,F元素在地壳中含量居第二位;A与B、C、D分别构成电子数相等的分子Q、X、Y;化合物AG在空气中与X反应产生白烟Z。
请回答下列问题:
G的原子结构示意图为 ,A2D2电子式为 ,
BD2的结构式为 ,Q的分子空间结构为 。
(2)固体Z为 晶体(填晶体类型),Z中所含化学键类型有 。
(3)在D同主族元素氢化物中,Y的沸点反常,原因是 。
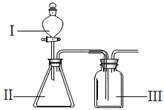
(4)B、F、G元素非金属性由强到弱的顺序为 ,若用下图装置验证这三种元素非金属性强弱,则在装置中加入的试剂分别为:Ⅰ ,Ⅱ ,Ⅲ 。(填化学式)
(1)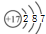 ,
,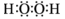 ,O=C=O,正四面体形。(2) 离子晶体, 离子键 极性键 (配位键) 。
,O=C=O,正四面体形。(2) 离子晶体, 离子键 极性键 (配位键) 。
(3)原因是 H2O分子间存在氢键 ;
(4) Cl 、C 、Si;ⅠHClO4;ⅡNa2CO3或NaHCO3;Ⅲ Na2SiO3
题目分析:根据题意可得:A是H;B是C;C是N;D是O;E是F是Si;G是Cl;Q是CH4;X是NH3;Y是H2O;Z是NH4Cl。(1)Cl的原子结构示意图为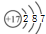 ; H2O2电子式为
; H2O2电子式为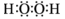 ; CO2的结构式为O="C=O;" CH4的分子空间结构为正四面体形.C在正四面体几何中心,四个H原子在四面体的顶点上。(2)固体NH4Cl为离子晶体,在该晶体中含有离子键、极性共价键、配位键。(3)在O同主族元素氢化物中,H2O是液态,而H2S、H2Se都是气态,水的沸点反常,原因是是在H2O的分子之间除了存在分子间作用力外,分子间存在氢键 ;(4)C、Si是同一主族的元素,从上到下,元素的非金属性逐渐减弱,所以非金属性C>Si;元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,酸性HClO4>H2CO3.所以非金属性Cl>C。因此元素的非金属性:Cl > C > Si。若用图示装置验证这三种元素非金属性强弱,则应该利用强酸制取弱酸的。在装置中加入的试剂分别为Ⅰ中HClO4;Ⅱ中Na2CO3或NaHCO3;Ⅲ 中Na2SiO3。
; CO2的结构式为O="C=O;" CH4的分子空间结构为正四面体形.C在正四面体几何中心,四个H原子在四面体的顶点上。(2)固体NH4Cl为离子晶体,在该晶体中含有离子键、极性共价键、配位键。(3)在O同主族元素氢化物中,H2O是液态,而H2S、H2Se都是气态,水的沸点反常,原因是是在H2O的分子之间除了存在分子间作用力外,分子间存在氢键 ;(4)C、Si是同一主族的元素,从上到下,元素的非金属性逐渐减弱,所以非金属性C>Si;元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,酸性HClO4>H2CO3.所以非金属性Cl>C。因此元素的非金属性:Cl > C > Si。若用图示装置验证这三种元素非金属性强弱,则应该利用强酸制取弱酸的。在装置中加入的试剂分别为Ⅰ中HClO4;Ⅱ中Na2CO3或NaHCO3;Ⅲ 中Na2SiO3。
