有A、B、C、D、E五种元素,原子序数依次增大,位于不同的三个短周期,其中B与D为同一主族元素,它们可形成化合物DB2、DB3,在同周期元素中,C的金属性最强,E的非金属性最强;请回答:
(1)写出A、E三种元素的名称:A____________,E_____________。
(2)A、B形成的原子个数比为1∶1的化合物的电子式为__________________,该化合物与DB2化合生成一种强酸的化学方程式为:__________________________。
(3)已知在一定条件下1mol DB2完全转化为气态DB3,放出98.3 kJ的热量。该反应的热化学方程式是
_____________________________,工业上进行这一反应的设备是_____________,反应的适宜条件为
________________________。
(4)用铂作电极电解由C、E形成化合物的饱和溶液时,检验阳极产物的实验方法为________________________________________;电解一段时间后,将阳极产物和阴极溶液混合,反应的离子方程式是
_____________________________。工业实际中常采用阳离子交换膜电解槽进行电解,若某一电极由碳钢网制成,则该电极为电解槽的___________(填“阴”或“阳”,下同)极,精制的由C、E形成的化合物的饱和溶液进入_________极室。
(1)氢;氯
(2)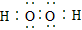 ;H2O2+SO2=H2SO4
;H2O2+SO2=H2SO4
(3)2SO2(g)+O2(g) 2SO3(g),ΔH=-196.6 kJ/mol;接触室;常压、400~500℃、催化剂;用湿润的
2SO3(g),ΔH=-196.6 kJ/mol;接触室;常压、400~500℃、催化剂;用湿润的
KI淀粉试纸接近阳极产物,试纸变蓝;Cl2+2OH-==Cl-+ClO-+H2O;阴;阳

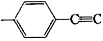 -CH3的分子结构,下列说法正确的是 [ ]
-CH3的分子结构,下列说法正确的是 [ ]