问题
单项选择题
患者,男,7岁,2天前出现发热、呕吐、剧烈头痛,3h前加重,神志不清。查体:有脑膜刺激征,意识障碍,眼底检查视盘水肿不明显。外周WBC4.5×10/L,HGB155g/L,PLT270×10/L;脑脊液检查:外观微混,白细胞110×10/L,淋巴细胞为83%,中性粒细胞17%;蛋白质0.64g/L,葡萄糖3.6mmol/L,氯化物122mmol/L;脑脊液沉淀物涂片,分别用墨汁、革兰染色和抗酸染色均未发现异常。该患者的初步诊断最可能是()
A.化脓性脑膜炎
B.结核性脑膜炎
C.病毒性脑膜炎
D.新型隐球菌脑膜炎
E.脑肿瘤
答案
参考答案:C

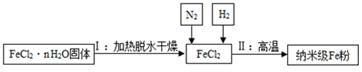
 Fe+2HCl
Fe+2HCl