问题
推断题
A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,C的非金属性最强,A、D同主族 隔周期,E元素原子最外层的p亚层电子数是s亚层电子数的一半。A、B能形成两种液态化合物甲和乙,原子个数比分别为2:1和1:1。根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性共价键的物质的电子式是______, C元素在周期表中的位置是_______。
(2)C和D的离子中,半径较小的是____(填离子符号)。
(3)将D的单质投入甲中,待D消失后再向上述溶液中加入E的单质,此时发生反应的化学方程式是____。
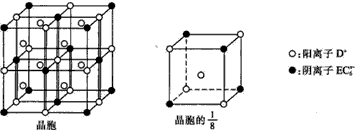
(4)C、D、E可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用O表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是________。
答案
(1) 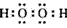 ;第二周期、第ⅦA族
;第二周期、第ⅦA族
(2) Na+
(3) 2Al+2NaOH+2H2O=2NaAlO2+3H2
(4) Na3AlF6
