我国是氧化铝生产大国,工业上每生产1 t氧化铝将排出1~2 t赤泥,赤泥大量堆积会对环境造成严重污染。赤泥中主要成分及含量:CaO约占46%、SiO2约占22%、Al2O3约占7%、Fe2O3约占11%、TiO2约占5%及少量其他物质。
⑴一种利用废弃赤泥的方法是将赤泥配成一定的液固比,作为一种吸收剂,吸收热电厂排放的含SO2的烟气,写出吸收SO2时可能发生的化学反应方程式 ▲ 。
⑵为综合利用赤泥中的各种成分,某科研小组设计了如下工艺流程:
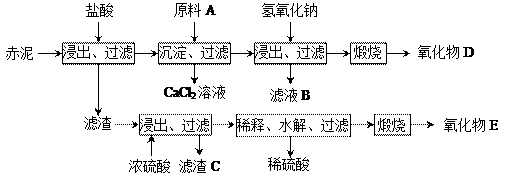 |
已知:TiO2不溶于稀盐酸、稀硫酸,能溶于浓硫酸生成TiOSO4(硫酸氧钛,易水解)。
①氧化物D的化学式是 ▲ ,原料A最好是下列物质中的 ▲ 。
A.氨水
B.氢氧化钠
C.生石灰
D.双氧水②写出上述工艺中投入氢氧化钠时反应的离子方程式 ▲ 。
③写出上述工艺中稀释时发生水解反应的化学方程式 ▲ 。
⑴CaO+SO2=CaSO3 或Ca(OH)2+SO2=CaSO3+H2O
⑵①Fe2O3 C
②OH-+Al(OH)3=AlO2-+2 H2O
③TiOSO4+2H2O=TiO(OH)2↓+H2SO4或TiOSO4+2H2O=TiO2·H2O↓+H2SO4
