X、Y、Z是中学化学常见的三 种元素,其中,X、Z位于短周期。常温下,X单质为黄绿色气体;向含Y离子的溶液中滴加氢氧化钠溶液,生成白色絮状沉淀,迅速变为灰绿色,最后变为红褐色;Z的最外层电子数与核外电子总数之比为3:13。请回答下列问题:
(1)Z在元素周期表中的位置是_________ ,X单质分子的电子式是_________。
(2)Z单质与Y的氧化物在高温条件下反应是冶炼Y单质的一种方法,该反应的化学方程式是___________。
(3)含上述元素的某些物质常用于处理工业废水,部分流程如下图:
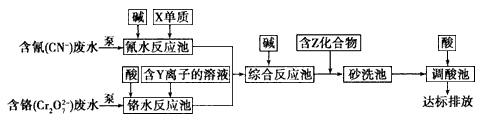
①处理含铬废水时,在反应池中Cr2O72-变为Cr3+,当反应转移1 mol电子时,有____________ mol Cr2O72-转化(计算结果保留两位小数)。
②含Z化合物可以使水中的悬浮颗粒发生凝聚,原因是 ______________(用文字和化学方程式表示)。
③处理含氰废水时,CN-最终转化为两种无毒气体,该反应的离子方程式是_______________。
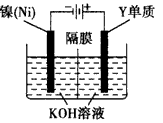
(4)利用下图装置电解可得到一种新型净水剂K2YO4,阳极的电极反应式为______________。
(1)第3周期ⅢA族;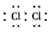
(2) Fe2O3 + 2 Al  Al2O3 +3Fe或 3Fe3O4 +8Al
Al2O3 +3Fe或 3Fe3O4 +8Al  4Al2O3+9Fe
4Al2O3+9Fe
或3FeO +2Al Al2O3 + 3Fe
Al2O3 + 3Fe
(3)①0.17
②Al3+ + 3H2O 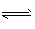 Al(OH)3(胶体)+3H+,氢氧化铝胶体能吸附水中的悬浮颗粒,使之沉淀下来
Al(OH)3(胶体)+3H+,氢氧化铝胶体能吸附水中的悬浮颗粒,使之沉淀下来
③2CN - +5Cl2 +8OH- ==2CO2 + N2 +4H2O + 10Cl-
(4)Fe-6e- +8OH- == FeO42- + 4H2O
