(15分)海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量的氯化钠,氯化钠中的金属元素位于元素周期表第__________族。
(2)目前国际上使用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是____________(填物理变化或化学变化)。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应式为食盐+H2O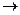 NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是____________。利用电解所得气体制36.5%的浓盐酸1 000 t,最少需要消耗食盐____________t。
NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是____________。利用电解所得气体制36.5%的浓盐酸1 000 t,最少需要消耗食盐____________t。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
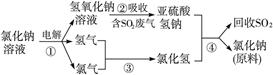
写出②④的化学反应方程式:____________________________________________。
上述亚硫酸氢钠与甲醛经过一定反应可以合成俗称“吊白块(雕白粉)”的物质。因吊白块对人体有害,不能用于食品漂白。其结构简式为HOCH2SO3Na,根据其结构特点,吊白块能发生的反应有____________。
A.皂化反应
B.聚合反应
C.与金属钠反应
D.氧化反应
(1)ⅠA
(2)物理变化
(3)NaCl 585
(4)NaOH+SO2====NaHSO3 HCl+NaHSO3====NaCl+H2O+SO2↑
(5)CD
(1)Na元素位于第3周期、第ⅠA族,注意不能写成第一族。蒸馏是通过加热使水的状态发生变化,是物理变化。电解饱和食盐水的反应为2NaCl+2H2O====2NaOH+H2↑+Cl2↑,生成物H2和Cl2反应:H2+Cl2 2HCl,综合两个反应得:NaCl~HCl,需要NaCl的质量为
2HCl,综合两个反应得:NaCl~HCl,需要NaCl的质量为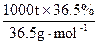 ×58.5 g·mol-1="585" t。“吊白块”中含有—OH(羟基),能与金属Na反应,也能发生氧化反应。
×58.5 g·mol-1="585" t。“吊白块”中含有—OH(羟基),能与金属Na反应,也能发生氧化反应。
