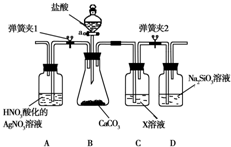
某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验).
实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸.
Ⅱ.A中看到白色沉淀时,…,关闭活塞a.
请回答:
(1)B中反应的离子方程式是______.
(2)通过步骤Ⅰ得知盐酸具有的性质是______(填字母).
A.挥发性 B.还原性 C.氧化性 D.酸性
(3)C装置的作用是______,X是______(写化学式).
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是______,D中反应的化学方程式是______.
(5)碳、硅的非金属性逐渐减弱的原因是______(从原子结构角度加以解释).
(1)B中发生盐酸与碳酸钙的反应,生成氯化钙、水、二氧化碳,该离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(2)A中看到白色沉淀,盐酸能与盐反应,可知盐酸具有的酸性、挥发性,故答案为:AD;
(3)X为碳酸氢钠溶液,与挥发的盐酸反应,可除去二氧化碳中混有的HCl,C装置的作用是除HCl气体,
故答案为:除HCl气体;NaHCO3;
(4)D中发生二氧化碳与硅酸钠溶液的反应,该反应为Na2SiO3+CO2+H2O=H2SiO3(胶体)+Na2CO3,步骤Ⅱ中未写的操作和现象是关闭弹簧夹1,打开弹簧夹2,当D中出现白色胶状沉淀后,
故答案为:关闭弹簧夹1,打开弹簧夹2,当D中出现白色胶状沉淀后;Na2SiO3+CO2+H2O=H2SiO3(胶体)+Na2CO3;
(5)碳、硅的非金属性逐渐减弱的原因是碳和硅位于同一主族,从上到下,原子半径逐渐增大,得电子的能力减弱,非金属性减弱,故答案为:碳和硅位于同一主族,从上到下,原子半径逐渐增大,得电子的能力减弱,非金属性减弱.

 式中标有ad的物质表示吸附在金属铂表面的原子或分子,对上述反应过程的下列说法有错误的是[ ]
式中标有ad的物质表示吸附在金属铂表面的原子或分子,对上述反应过程的下列说法有错误的是[ ]