图表法、图象法是常用的科学研究方法.

(1)I.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第______族.
II.图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第______族元素氢化物的沸点的变化规律.不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是a还是b?并说出理由:______.
(2)部分有机物的熔沸点见下表:
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 |
|
|
|
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
(1)I.电离能是元素的原子失去电子所需要的能量,根据图象可以知道,元素的第三电离能之后数据相当大,说明易失去三个电子,最外层电子数为3,故为第ⅢA的元素,故答案为:IIIA;
II.图B中元素的氢化物的沸点变化规律的图象中,折线c可以得出该族元素的氢化物的沸点随着原子序数的递增,从上到下是逐渐升高的,符合第IVA元素的性质,没有特例出现,A点所示的氢化物是水,在水中,由于在水分子间存在氢键,其沸点高于氧族元素中的其它氢化物的沸点,即曲线b符合要求,故答案为:b;A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点;
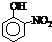
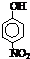
(2)根据表中所给的物质可以看出:前三种和后四种物质均是互为同系物,发现同系物相对分子质量越大、分子间作用力越强,沸点越高,并且是当有机能形成分子内氢键时,分子间作用力减弱,熔点变低;当分子间能形成氢键时,分子间作用力增强,熔点升高,故答案为:同系物相对分子质量越大、分子间作用力越强,故沸点越高;当有机能形成分子内氢键时,分子间作用力减弱,熔点变低(当分子间能形成氢键时,分子间作用力增强,熔点升高).