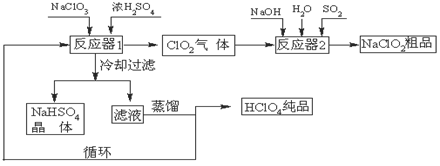
(12分)工业上生产高氯酸(沸点:90oC)时还同时生产了亚氯酸钠,其工艺流程如下:
(1)冷却过滤的目的是降低NaHSO4的 并分离出NaHSO4晶体。
(2)反应器2中发生反应的离子方程式为 。SO2的作用是作 剂。
(3)循环使用的物质是 。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是 。
(5)工业上用铂作阳极、铜或银作阴极电解盐酸也可制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现) 。
(12分)(1)溶解度(2分)(2)2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O;(2分)还原(2分)
(3)H2SO4(2分) (4)高氯酸的沸点比较低,容易从溶液中逸出;(2分)
(5)阳极反应式 HCl+ 4H2O -8e—= HClO4 + 8H+。(2分)
(1)溶解度 NaHSO4的溶解度随温度的升高而增大,随温度的降低而减小。冷却后更易析出NaHSO4晶体。
(2)2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O
在反应中由的SO2硫元素由+4价到+6价,失去电子,为还原剂
(4)蒸馏时,物质按沸点由低到高依次被蒸馏出。高氯酸的沸点为90 oC,很容易蒸出
(5)根据电解池原理,阳极物质失去电子,化合价升高,被氧化
