阅读理解。
Komal loved playing baseball very much. She always wanted to be a baseball player in her school team. She
practiced nearly every day, even on rainy days. Her grandfather lived in another city. He was a great baseball
player. So she sent a postcard to him saying, "When you come here for holiday, would you like to teach me how
to play baseball better?" The next week she got his letter saying, "Sorry, I'm very busy now." Komal was so sad.
But in fact, his grandpa decided to go. He didn't tell Komal the truth (真 相) because he wanted to give her a
surprise.
When the door bell rang on Saturday morning, Komal was so surprised to see her grandfather when she opened
the door. Grandfather brought Komal a baseball as a present. It was the one he used in one of the Olympic Games.
Komal was very happy and put it on her bookshelf. With the grandfather's help, Komal improved a lot and became
a player of the school team in the end.
根据短文内容,回答问题.
1. What sports was Komal fond of?
_____________________________________
2. What did Komal's grandfather do?
_____________________________________
3. Did Komal's grandfather go to Komal's home at last?
_____________________________________
4. Where did Komal put the present her grandfather gave her?
_____________________________________
5. What was Komal's dream?
_____________________________________
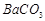 、
、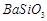 、
、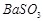 、
、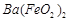 等]。某化工厂主要生产
等]。某化工厂主要生产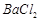 、
、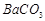 、
、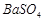 ,现利用钡泥制取
,现利用钡泥制取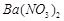 ,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3 (2)Fe3+在pH=3.7时即可水解即沉淀完全)
,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3 (2)Fe3+在pH=3.7时即可水解即沉淀完全)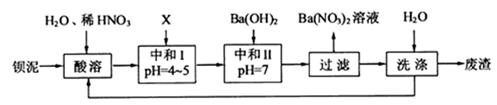
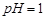 ,
,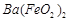 与
与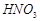 的反应化学方程式为:
的反应化学方程式为: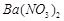 溶液中得到其晶体的分离方法叫 。
溶液中得到其晶体的分离方法叫 。