有A、B、C、D、E五种短周期元素,原子序数依次增大,元素A的一种原子无中子,元素B和C都有2个电子层,它们能生成无色无味的气体BC2.元素C能与A生成两种化合物,D元素与A元素属于同一主族,元素E的单质能与BC2反应,且它的最高价氧化物对应的水化物呈碱性.试回答:
(1)B的元素名称是______,D的原子结构示意图是______.
(2)写出BC2的电子式______.
(3)写出C2转化C3的化学反应方程式为:______.
(4)写出下列化学反应方程式:
①E与BC2:______.
②D2C2与BC2:______.
A、B、C、D、E五种短周期元素,原子序数依次增大.元素A的一种原子无中子,则A为氢元素;D元素与A元素属于同一主族,D的原子序数比A至少大3,故D为Na元素;元素B和C都有2个电子层,它们能生成无色无味的气体BC2,该无色无味的气体可能为CO2,则可能B为碳元素、C为氧元素;氧元素能与氢元素生成水与过氧化氢两种化合物,符合题意.元素E的单质能与CO2反应,且它的最高价氧化物对应的水化物呈碱性,则E为金属,应为Mg元素,
(1)由上述分析可知,B为碳元素;D为Na元素,钠原子核外电子数为11,有3个电子层,由里到外各层电子数分别为2、8、1,钠的原子结构示意图是
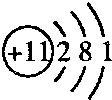
,
故答案为:碳;
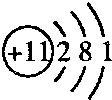
;
(2)CO2分子中碳原子与氧原子之间形成2对共用电子对,电子式为
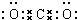
,
故答案为:
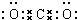
;
(3)O2转化O3的化学反应方程式为:3O2
2O2, 放电 .
故答案为:3O2
2O2; 放电 .
(4)①Mg在CO2中燃烧生成氧化镁与碳,反应方程式为2Mg+CO2
2MgO+C, 点燃 .
故答案为:2Mg+CO2
2MgO+C; 点燃 .
②Na2O2与CO2反应生成碳酸钠与氧气,反应方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2.
