下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)地壳中含量最多的金属元素是______.
(3)写出②与④形成的化合物的电子式______.
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______.
(5)写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:______.
(6)写出⑤与氢氧化钠溶液反应的化学方程式:______.
由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为Cl,⑧为Ar,⑨为K,⑩为Br,
(1)以上元素中只有Ar的最外层电子数为8,性质不活泼,最稳定,其原子结构示意图为

,故答案为:

;
(2)地壳中元素的含量较多的有O、Si、Al、Ca,则金属元素最多的为Al,故答案为:Al;
(3)②与④形成的化合物为MgF2,为离子化合物,其电子式为
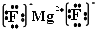
,故答案为:
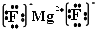
;
(4)以上元素中最高价氧化物对应的水化物中酸性最强的为HClO4,碱性最强的为KOH,呈两性的氢氧化物为Al(OH)3,故答案为:HClO4;KOH;Al(OH)3;
(5)⑤的氢氧化物为Al(OH)3,与NaOH溶液反应的离子反应为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(6)⑤为Al,与NaOH溶液反应生成偏铝酸钠和氢气,反应为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
