下表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是______,酸性最强的是______;
(3)E单质的结构式为______; D元素最高价氧化物的电子式为______;
(4)写出B与C两元素最高价氧化物的水化物之间反应的离子方程式______.
(1)根据元素周期表的结构,表中A、B、C、D、E、F、G、H、I元素分别是H、Na、Al、C、N、P、F、Cl、Ne,则其中Na和Al是金属元素,根据同周期元素金属性递变规律可知,金属性最强的应该是Na,即还原性最强的单质是Na;其中H、C、N、P、F、Cl是非金属元素,根据同周期、同主族元素非金属性递变规律可知,非金属性最强的应该是F,即氧化性最强的单质是F2;化学性质最不活泼的应是惰性气体,即Ne.故答案为:Ne;F2;Na;
(2)由(1)分析,金属性最强的是Na,最高价氧化物的水化物碱性最强的是NaOH;非金属性最强的是F,但是F无最高正价,则酸性最强的是应是HClO4.,故答案为:NaOH;HClO4;
(3)E的单质是N2,其结构式是N三N;D元素最高价氧化物是CO2,其电子式为:
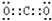
,故答案为:N三N;
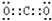
;
(4)B与C两元素最高价氧化物的水化物分别是NaOH和Al(OH)3,二者反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O.
