问题
问答题
为了比较硫与碳的非金属性的强弱,某同学想通过比较两种元素的最高价氧化物对应的水化物的酸性强弱来证明硫与碳的非金属性的强弱,采用下图中的甲、乙装置进行探究,请你帮助他完成下列问题:
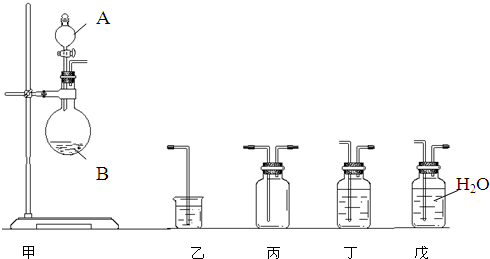
(1)仪器A中应盛放的药品是______,仪器B中应盛放的药品是______,装置乙中应盛放的药品是______.
(2)B中发生反应的离子方程式为:______;在装置乙中观察到的现象是:______.
(3)该实验能证明硫与碳的非金属性的强弱的理论依据是:______.
答案
(1)比较C、S元素的最高价氧化物对应的水化物的酸碳酸和硫酸的酸性强弱来证明硫与碳的非金属性的强弱所需进行的反应是硫酸和碳酸盐的反应,强酸可以制得弱酸,所以可以在A中放稀硫酸,在B中放碳酸盐,可用澄清的石灰水来证明二氧化碳的生成,进而确定硫酸可以和可溶性的碳酸盐反应生成碳酸,
故答案为:稀H2SO4;Na2CO3(或可溶性碳酸盐);澄清石灰水;
(2)硫酸和可溶性的碳酸盐反应的实质是:CO32-+2H+=CO2↑+H2O,二氧化碳可以使石灰水变浑浊,
故答案为:CO32-+2H+=CO2↑+H2O;澄清石灰水变浑浊;
(3)根据硫酸可以和可溶性的碳酸盐反应可以知道硫酸酸性强于碳酸,而元素的最高价氧化物对应的水化物的酸性越强说明该元素的非金属性越强,
故答案为:由H2SO4制H2CO3即由强酸制弱酸,S的最高价氧化物对应水化物的酸性强,故S的非金属性比C强.
