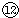问题
填空题
如表是元素周期表的一部分:
| 族
| I A | II A | III A | IV A | V A | VI A | VII A |
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
|
|

的氢化物的还原性______稳定性______(填强或弱)
(2)某元素的原子结构示意图为:

,在周期表位于______.该氢化物沸点比甲烷______.
(3)用电子式表示

与⑧形成化合物形成过程:______.
(4)写出⑦与⑨、⑨与
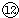
的最高价氧化物对应水化物反应的离子方程式:⑦与⑨:______、⑨与
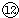
______.
答案
(1)⑩为P,其氢化物的化学式为PH3,
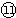
为S,非金属性S>P,则还原性PH3>H2S,气态氢化物H2S>PH3,故答案为:PH3;强;弱;
(2)K层电子数最多为2,则x=2,则原子结构中有3个电子层,最外层电子数为4,在元素周期表中的位置为第三周期第ⅣA族,气态氢化物的相对分子质量PH3>CH4,则PH3沸点高,
故答案为:第三周期第ⅣA族;高;
(3)
为S,⑧为Mg,形成的化合物为离子化合物,其形成过程为
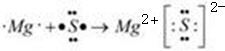
,故答案为:
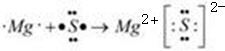
;
(4)⑦为Na,⑨为Al,

为Cl,NaOH与Al(OH)3反应的离子反应为OH-+Al(OH)3═AlO2-+2H2O,HClO4与Al(OH)3反应的离子反应为3H++Al(OH)3═Al3++3H2O,
故答案为:OH-+Al(OH)3═AlO2-+2H2O;3H++Al(OH)3═Al3++3H2O.