问题
问答题
某实验室的废水中含有大量AgNO3、Zn(NO3)2和Fe(NO3)2,课外小组同学欲从该废液中回收银,并得到副产品硫酸亚铁晶体.实验方案如下:
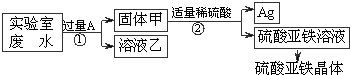
(1)固体甲中含有的物质是(填化学式)______;溶液乙的化学式为______.
(2)写出步骤①的化学方程式:______.
(3)检验步骤①向废水中加入A是否过量的方法是______.
答案
(1)根据流程可知①中加入的为铁粉,铁能与溶液中的硝酸银反应,得到金属银及过量未完全反应的铁;硝酸银被过量的铁完全反应,锌排在铁的前面,因此溶液中含有不与铁反应的硝酸锌,以及反应后生成和原溶液中就含的硝酸亚铁;
故答案为:Fe、Ag;Zn(NO3)2、Fe(NO3)2;
(2)铁的活动性比银强,加入的铁粉与混合溶液中的硝酸银反应,生成硝酸亚铁和银;
故答案为:Fe+2AgNO3═2Ag+Fe(NO3)2;
(3)加入A过量时,所得固体甲中含有因加入过量而未完全反应的铁,因此可取固体加入稀硫酸或稀盐酸,观察是否有气泡放出,有气泡则固体甲中含铁,加入的铁过量;
故答案为:取少量固体甲于试管中,加入稀硫酸或稀盐酸,有气泡冒出,则加入的铁过量.

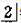 锥形牙,与邻牙之间约1mm间隙,下列修复方法中不宜采用的是()。
锥形牙,与邻牙之间约1mm间隙,下列修复方法中不宜采用的是()。