问题
填空题
(6分)稀硝酸和足量的铁反应的化学方程式如下:
3Fe + 8HNO3 = 3Fe(NO3)2+ 2NO↑+ 4H2O
(1)该氧化还原反应的氧化剂是 ,氧化产物是 。
(2)请用双线桥法表示出电子转移的方向和数目:
3Fe +8HNO3 = 3Fe(NO3)2+2NO↑+4H2O
(3)若生成标准状况下11.2LNO气体,反应中被还原的HNO3的物质的量为________。
答案
(共6分) (1)HNO3; Fe(NO3)2 (各1分)
(2)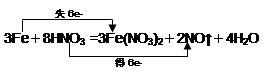 (2分)
(2分)
(3)0.5 mol (2分)
题目分析:(1)根据反应放热化学方程式可知,铁元素的化合价从0价升高到+2价,失去2个电子;硝酸中氮元素的化合价从+5价降低到+2价,得到3个电子,所以硝酸是氧化剂,硝酸亚铁是氧化产物。
(2)根据电子的得失守恒可知,用双线桥法表示出电子转移的方向和数目为
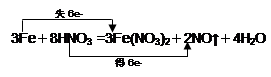
(3)硝酸的还原产物是NO,物质的量是11.2L÷22.4L/mol=0.5mol,所以根据氮原子守恒可知,被还原的硝酸的物质的量是0.5mol。
点评:本题是高考中的常见考点之一,试题难易适中,侧重能力的考查。氧化还原反应判断的关键是准确标出有关元素的化合价变化情况,然后根据有关概念判断即可。而氧化还原反应的计算,则一般利用电子的得失守恒进行。
