Ⅰ.已知a、b、c、d、e为短周期主族元素.其中
①a和b属同周期元素,二者能形成多种气态化合物;
②a和c属同周期元素,二者能形成两种气态化合物;
③a和d属同主族元素,二者能形成两种常见化合物;
④e可分别和a、b、c、d形成具有相同电子数的共价化合物甲、乙、丙、丁.
请回答:
(1)a元素为______,甲的分子式为______,丁的电子式为______.
(2)由上述一种或几种元素形成的物质可与水发生氧化还原反应但不属于置换反应,写出一个符合要求的化学反应方程式:______.
Ⅱ.碳和碳的化合物在人类生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.
(1)甲烷燃烧时放出大量的热,可作为能源应用于人类的生产和生活.
已知①2CH4(g)+3O2(g)═2CO(g)+4H2O(l);△H1=-1214.6kJ/mol;
②CO2 (g)═CO (g)+
O2(g);△H2=+283kJ/mol1 2
则甲烷燃烧热的热化学方程式为______.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②该反应的正反应为______(填“吸”或“放”)热反应;
③若要使实验3达到平衡状态时各物质的体积分数与实验2分别相等,则a、b应满足的关系是______(用含a、b表示).
Ⅰ.已知a、b、c、d、e为短周期主族元素.①a和b属同周期元素,二者能形成多种气态化合物,②a和c属同周期元素,二者能形成两种气态化合物,据此可知a为O元素,b为N元素,c为C元素;③a和d属同主族元素,二者能形成两种常见化合物,d为S元素;④e可分别和a、b、c、d形成具有相同电子数的共价化合物甲、乙、丙、丁,为18电子化合物,e为H元素,故甲为H2O2,乙为N2H4,丙为C2H6,丁为H2S.
(1)由上述分析可知,a为氧元素;甲为H2O2;丁为H2S,电子式为
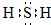
,故答案为:氧;H2O2;
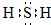
;
(2)由上述一种或几种元素形成的物质可与水发生氧化还原反应但不属于置换反应,符合要求的化学反应方程式:3NO2+H2O=NO+2HNO3等,
故答案为:3NO2+H2O=NO+2HNO3;
Ⅱ.(1)已知①2CH4(g)+3O2(g)═2CO(g)+4H2O(l);△H1=-1214.6kJ/mol;
②CO2 (g)═CO (g)+
O2(g);△H2=+283kJ/mol,1 2
根据盖斯定律,①-②×2得2CH4(g)+4O2(g)═2CO2(g)+4H2O(l);△H=-1780.66kJ/mol;
所以甲烷燃烧热的热化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(l)的△H=-890.3 kJ/mol,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)的△H=-890.3 kJ/mol;
(2)①由表中数据可知,平衡时n(CO2)=1.6mol,所以v(CO2)=
=0.16mol/(L•min),根据速率之比等于化学计量数之比,所以v(H2)=v(CO2)=0.16mol/(L•min),故答案为:0.16;1.6mol 2L 5min
②反应各组分的化学计量数为1,故可以用物质的量代替浓度计算平衡常数.
650℃时到达平衡:H2O(g)+CO(g)⇌CO2(g)+H2(g),
开始(mol):2 4 0 0
变化(mol):1.6 1.6 1.6 1.6
平衡(mol):0.4 2.4 1.6 1.6
所以650℃的平衡常数k=
=1.6×1.6 0.4×2.4 8 3
900℃时到达平衡:H2O(g)+CO(g)⇌CO2(g)+H2(g),
开始(mol):1 2 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):0.6 1.6 0.4 0.4
所以900℃的平衡常数k=
=0.4×0.4 0.6×1.6
.1 6
升高温度平衡常数减小,即升高温度平衡向逆反应移动,升高温度向吸热反应移动,故正反应为放热反应,
故答案为:放;
③使实验3达到平衡状态时各物质的体积分数与实验2分别相等,为等效平衡,该反应为反应前后气体的体积不发生变化,满足n(H2O):n(CO)=1:2即可,即b=2a.
故答案为:b=2a.
