问题
问答题
有一固体混合物A,已知其中可能含有Ca(OH)2、NaOH、Na2CO3三种物质中的两种或三种.按照下图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行).
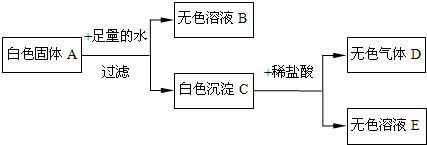
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体D的化学式为______.
(2)在混合物A里一定存在的物质有______(填化学式).
(3)在溶液B中,一定大量存在的阴离子是______(写离子符号).
(4)写出白色沉淀C跟盐酸反应的化学方程式:______.
答案
Ca(OH)2、NaOH、Na2CO3三种物质中氢氧化钙和碳酸钠反应可以生成碳酸钙沉淀,所以混合物中一定含有Ca(OH)2、Na2CO3;而碳酸钙能够和盐酸反应生成二氧化碳和氯化钙及水,所以C是碳酸钙、D是二氧化碳、E是氯化钙溶液;
(1)气体D是二氧化碳;
(2)由分析知混合物中一定含有Ca(OH)2和Na2CO3;
(3)由于Ca(OH)2、Na2CO3反应可以生成碳酸钙和氢氧化钠,所以B溶液中含有的阴离子是Na+;
(4)白色沉淀C跟盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
故答案为:(1)CO2;(2)Ca(OH)2和Na2CO3;(3)Na+;(4)CaCO3+2HCl═CaCl2+H2O+CO2↑;
