下表为周期表前20号元素中某些元素的有关数据:
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.86 | 1.52 | 0.66 | 1.43 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
| 最高价态 | +1 | +1 | -- | +3 | +4 | +5 | +7 | +1 | +5 | -- |
| 最低价态 | -- | -- | -2 | -- | -4 | -3 | -1 | -- | -3 | -1 |
(1)写出⑦⑨与氢元素形成的常见离子化合物的电子式______
(2)上述⑤、⑥、⑦号元素中某2种元素形成的化合物中,每一个原子都满足最
外层为8电子稳定结构的物质可能是______、______;
(3)某元素R的原子半径为1.04×10-10m,该元素在周期表中的位置是______
(4)以上10种元素的原子中,失去核外第一个电子所需能量最少的是______
(5)④、⑦、⑧、⑩四种元素形成的离子,其半径由小到大的顺序为______.
元素的最高正价=最外层电子数=族序数,同主族元素原子,从上到下原子半径逐渐增大,故⑩为F,⑦为Cl,①为Na,②为Li,⑧为K,同周期元素的原子,从左到右原子半径逐渐减小,③无最高价,最低价为-2,故为O,④的半径比钠小,比Si大,最外层电子数为3,应为Al,⑤的半径比O大,最外层电子数为4,故为C,⑥的半径比Cl大,最外层电子数为,应为P,⑨的半径介于C和O之间,应为N,
(1)氯元素、氮元素与氢元素形成的常见离子化合物为氯化铵,电子式为:
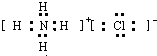
,故答案为:
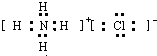
;
(2)|元素化合价|+元素原子的最外层电子数=8,则原子就满足最外层为8电子的稳定结构,C、Cl、P中某2种元素形成的化合物中,只有CCl4、PCl3符合等式,故答案为:CCl4、PCl3;
(3)1.04×10-10m介于1.10×10-10m和0.99×10-10m之间,即半径大小介于P和Cl之间,故为S,位于第三周期,第ⅥA族,故答案为:第三周期,第ⅥA族;
(4)锂、钠、钾的最外层只有一个电子,失一个电子的能力较强,其中K失电子能力最强,故失去核外第一个电子所需能量最少,故答案为:K;
(5)电子层越多半径越大,则F-<K+,对于具有核外电子数一样多的离子来说,核内质子数越多,半径越小,则Al3+<F-、K+<Cl-,故答案为:Al3+<F-<K+<Cl-.
