某研究性学习小组设计了一组实验来探究元素周期律.
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红色纸条.
已知常温下浓盐酸与高锰酸钾能反应生成氯气.
可选择的试剂有:大理石、碳酸钠粉末、浓盐酸、稀硝酸、硅酸钠溶液.
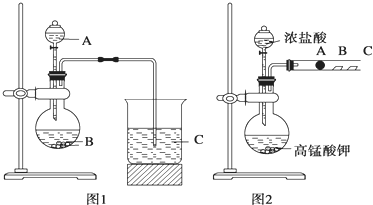
(1)甲同学实验中(图1):
①从给出试剂中选出最佳物质:A______,B______.(填化学式)
②烧杯C中发生反应的离子方程式为______.
(2)乙同学实验中(图2):
①写出A处反应的离子方程式______.
②B处实验现象是______.
③若高锰酸钾的还原产物为Mn2+,当有0.04mol高锰酸钾参加反应时,则可生成标准状况下的氯气的体积为______L.
(1)①验证元素非金属性与对应最高价含氧酸之间的关系,所选取的酸应为稀硝酸,圆底烧瓶内的固体药品应为大理石,不能用碳酸钠粉末,反应剧烈,不易控制反应,C中应盛装硅酸钠溶液,以此来证明硝酸、碳酸以及硅酸的酸性强弱,故答案为:HNO3;CaCO3;
②C中盛装硅酸钠溶液,由于碳酸酸性比硅酸强,在C中通入二氧化碳气体生成硅酸沉淀,
反应的离子方程式为CO2+SiO32-+H2O=H2SiO3↓+CO32-,故答案为:CO2+SiO32-+H2O=H2SiO3↓+CO32-;
(2)单质的氧化性Cl2>Br2>I2,则
①氯气通入溴化钠溶液中发生置换反应生成溴,反应的离子方程式为Cl2+2Br-=Br2+2Cl-,
故答案为:Cl2+2Br-=Br2+2Cl-;
②氯气和KI溶液反应生成单质碘,淀粉变蓝,故答案为:试纸变蓝;
③根据电子守恒可得关系式:2KMnO4~5Cl2,当有0.04mol高锰酸钾参加反应时,生成n(Cl2)=0.04mol×
=0.1mol,5 2
则V(Cl2)=0.1mol×22.4L/mol=2.24L,
故答案为:2.24.
