问题
填空题
【三选一—选修化学与技术】
羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料。其常用的制备方法有两种:
方法A:用浓氨水分别调节Ca(NO3)2和(NH4)2HPO4溶液的pH,使其约为12;在剧烈搅拌下,将
(NH4)2HPO4溶液 缓慢滴入Ca(NO3)2溶液中。
方法B:在剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。

3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O==Ca5(PO4)3OH↓+____ .
②5Ca(OH)2 +3H3PO4==___
(2)与方法A相比,方法B的优点是____
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是___
(4)图中所示3种钙盐在人体中最稳定的存在形式是___(填化学式)。
(5)糖沾在牙齿上,在酶的作用下产生酸性物质,易形成龋齿。结合化学平衡移动原理,分析其原因____
答案
(1)①10NH4NO3 +3H2O; ②Ca5(PO4)3OH+9H2O
(2)惟一副产物为水,工艺简单
(3)反应液局部酸性过大,会有CaHPO4、Ca3(PO4)2生成
(4)Ca5(PO4)3OH
(5)酸性物质使沉淀溶解平衡:Ca5(PO4)3OH(s)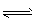 5Ca2+ (aq)+ 3PO43-(aq) +OH-(aq) 向右移动,导致
5Ca2+ (aq)+ 3PO43-(aq) +OH-(aq) 向右移动,导致
Ca5(PO4)3OH溶解,形成龋齿
