金属和非金属与人类生活、生产密不可分.
(1)我国多使用铁锅炒菜,铁锅在______条件下易生锈.
(2)清末铝制艺术品至今保存完好,艺术品未被锈蚀的主要原因是(填字母)______.
A.铝不易被氧化 B.铝的金属活动性比较弱 C.铝表面的氧化膜具有保护作用
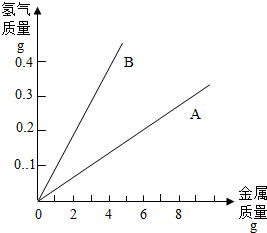
(3)图为金属与过量盐酸反应的关系图,其中A、B两条直线分别代表镁、铁、锌三种金属中的两种.
A代表的是(填元素符号)______;
写出B与盐酸反应的化学方程式______.
高纯硅是制造计算机电路芯片的主要原料.请回答:
(1)硅元素属于______填金属或非金属)元素,在地壳中硅元素的含量仅次于______元素.
(2)硅在氧气中燃烧生成二氧化硅,并放出大量的热,可作未来新能源,该反应的基本反应类型为______.
(3)工业上用石英(主要成分为SiO2)制备粗硅的反应为:SiO2+2C
Si+2R↑,则R的化学式为______,反应后硅元素的化合价______(填写“升高”或“降低”). 高温 .
(4)生产高纯硅可用三氯硅烷(SiHCl3).三氯硅烷在空气中极易燃烧,燃烧时可观察到有红色火焰和白色烟,生成物为二氧化硅、氯化氢和氯气,此反应的化学方程式为______.
(1)铁锅在潮湿的环境中容易生锈.故填:水和氧气存在的.
(2)铝制艺术品的外面有一层致密而坚硬的保护膜,对铝制品起到了保护作用.故填:C.
(3)镁、铁、锌与稀盐酸反应的化学方程式,镁、铁、锌与生成的氢气的质量比分别为:
Mg+2HCl═MgCl2 +H2↑,Fe+2HCl═FeCl2 +H2↑,Zn+2HCl═ZnCl2 +H2↑.
24 2 56 2 65 2
由金属与过量盐酸反应的关系图中可知,A中金属质量与生成氢气的质量比接近65:2,是锌;B中金属质量与生成氢气的质量比接近12:1,是镁.
A代表的是锌.故填:Zn.
镁与盐酸反应的化学方程式为:Mg+2HCl═MgCl2 +H2↑.
(1)硅属于非金属元素,在地壳中硅元素的含量仅次于氧元素.故填:非金属;氧.
(2)硅在氧气中燃烧生成二氧化硅,反应物是两种,生成物是一种,属于化合反应.故填:化合反应.
(3)根据质量守恒定律可知,每个R中含有1个碳原子和1个氧原子,是一氧化碳.故填:CO.
二氧化硅中,硅元素的化合价是+4,单质硅中,硅元素的化合价是0.反应后硅元素的化合价降低了.故填:降低.
(4)三氯硅烷在空气中燃烧时,能生成二氧化硅、氯化氢和氯气,反应的化学方程式为:SiHCl3+O2
SiO2 +HCl+Cl2. 点燃 .