问题
填空题
工业合成氨与制备硝酸一般可连续生产,流程如下
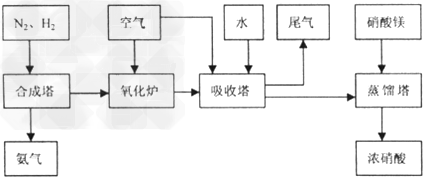
(1)工业生产时,制取氢气的一个反应为: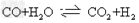 ,
,
①t℃时,往l L密闭容器中充入0.2 mol CO和0.3 mol水蒸气,反应建立平衡后,体系中c(H2)=0.12 mol/L,该温度下此反应的平衡常数K=________;(请填数字不必带单位)
②保持温度不变,向上述平衡体系中再加入0.1 mol CO,当反应重新建立平衡时,水蒸气的总转化率α(H2O)=__________。
(2)合成塔中发生反应为:N2(g)+3H2(g) 2NH3(g)下表为不同温度下该反应的平衡常数。由此可推知,表中T1_______573K(填“>”、“<”或“=”)。在生产中,若要增大H2的转化率,在其他条件不变的情况下可以采取的措施为________(填字母)。
2NH3(g)下表为不同温度下该反应的平衡常数。由此可推知,表中T1_______573K(填“>”、“<”或“=”)。在生产中,若要增大H2的转化率,在其他条件不变的情况下可以采取的措施为________(填字母)。
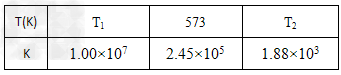
A.加入一定量H2 B.加入一定量N2
C.将生成的气体NH3液化分离 D.升高温度
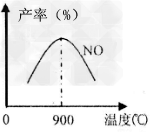
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3+5O2 4NO+6H2O △H=-905kJ/mol,不同温度下NO产率如图所示,温度高于900℃时,NO产率下降的原因______________________。
4NO+6H2O △H=-905kJ/mol,不同温度下NO产率如图所示,温度高于900℃时,NO产率下降的原因______________________。
(4)吸收塔中反应为:3NO2+H2O 2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因是___________________
2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因是___________________
答案
(1)①1;②50%
(2)<;BC
(3)温度高丁900℃时,平衡向左移动
(4)充入空气,NO转化为NO2,有利于提高原料利用率
