一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+ 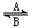 Fe3+。在过程A中,Fe2+作 剂。
Fe3+。在过程A中,Fe2+作 剂。
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有 性。
(3)某同学要检验Fe3+,向溶液中加入 (写化学式)溶液变成红色。要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 。
(5)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是 (填字母)
a.铜粉 b.氯气 c.铁粉 d.KSCN溶液
(8分)(1)还原(1分); (2)还原(1分);
(3)KSCN (1分) c (1分)
2Fe2++Cl2==2Fe3++2Cl‾(1分)
(4)2Fe3++Cu2+==2Fe2++Cu2+(1分)
(5)c (2分)
题目分析:(1)在A中铁元素的化合价由+2价升高到+3价,铁元素的化合价升高,则A中Fe2+做还原剂。
(2)由信息维生素C可使食物中的三价铁离子还原成二价铁离子,该反应中铁元素的化合价降低,则维生素C中某元素的化合价升高,即维生素C为还原剂,体现还原性。
(3)Fe3+和KSCN溶液发生特征反应,反应后溶液呈红色。氯化亚铁被强化剂氧化呈氯化铁,故选c。离子方程式为2Fe2++Cl2==2Fe3++2Cl‾。
(4)FeCl3 与金属铜发生氧化还原反应,铜溶解,反应的离子方程式为2Fe3++Cu2+==2Fe2++Cu2+。
(5)铁的活泼性大于铜的活泼性,置换出铜一般用铁,故选c。
点评:本题属于信息习题,考查氧化还原反应中氧化剂、还原剂及氧化性、还原性,明确元素的化合价变化来分析是解答本题的关键,难度中等。
