问题
问答题
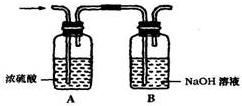
有一无色气体可能含有H2、CO、CH4 (以下称试验气体)中的一种或几种.为了确定其组成,将其充分燃烧,再把生成的气体依次通过如图所示的装置.
(1)若A装置的质量增加,B装置的质量不变,则试验气体为______,该气体燃烧的化学方程式是:______;
(2)若A装置的质量不变,B装置的质量增加,则试验气体为______,B瓶中发生反应的化学方程式是:______;
(3)若A装置和B装置的质量都增加,则试验气体的可能组成有:______.
答案
(1)装置A的质量增加,B装置的质量不变,说明有水生成,没有二氧化碳气体生成,实验气体是氢气.氢气燃烧的化学方程式是:2H2+O2
2H2O; 点燃 .
故答案为:H2;2H2+O2
2H2O. 点燃 .
(2)若A装置的质量不变,B装置的质量增加,说明有二氧化碳生成,没有水生成,则试验气体为一氧化碳.燃烧生成的二氧化碳,与B瓶中的氢氧化钠溶液反应,生成碳酸钠和水,反应的方程式是:CO2+2NaOH=Na2CO3+H2O.
故答案为:CO;CO2+2NaOH=Na2CO3+H2O.
(3)若A装置和B装置的质量都增加,说明既有二氧化碳生成,也有水生成,则试验气体的可能组成有:H2、CO、CH4 或H2、CO.
故答案为:H2、CO、CH4 或H2、CO.
