问题
问答题
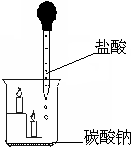
如图所示,向烧杯内Na2CO3粉末滴入盐酸,观察烧杯中燃着的小蜡烛.观察下面一支蜡烛的火焰先熄灭,上面一支随后熄灭.
(1)请写出碳酸钠与盐酸反应的化学方程式:______;
(2)从这个实验说明了CO2具有的性质是:
①:______;
②:______.
根据以上性质,得出CO2的用途之一是:______.
答案
(1)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+CO2↑+H2O;
(2)因为二氧化碳密度比空气大且不支持燃烧,所以下面的蜡烛先熄灭,然后上面的蜡烛才熄灭.可利用二氧化碳的这一性质进行灭火.
故答案为:(1)Na2CO3+2HCl═2NaCl+CO2↑+H2O
(2)①CO2即不能燃烧,也不能支持燃烧.②CO2的密度比空气大;灭火;
