问题
选择题
已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3 +6HCl=3Cl2+KCl +3H2O,
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
答案
答案:B
题目分析:A.②中生成物有单质但反应物没有单质,所以不是置换反应,A错误;B.①Cl2+2KBr=2KCl+Br2中氧化剂是氯气,氧化产物是溴,氯气的氧化性大于溴,②KClO3+6HCl=3Cl2+KCl+3H2O中氧化剂是氯酸钾,氧化产物是氯气,氯酸钾的氧化性大于氯气,③2KBrO3+Cl2=Br2+2KClO3中氧化剂是溴酸钾,氧化产物是氯酸钾,溴酸钾的氧化性大于氯酸钾,所以,氧化性强弱顺序是 KBrO3>KClO3>Cl2>Br2,B正确;C.②KClO3+6HCl=3Cl2+KCl+3H2O中,氧化剂是氯酸钾,还原剂是参加反应氯化氢的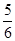 ,所以还原剂和氧化剂的物质的量之比是5:1,C错误;D.③还原剂是氯气,氧化剂是溴酸钾,该反应式中lmol还原剂反应则氧化剂得到电子的物质的量=2×(5-0)mol=10mol,D错误;
,所以还原剂和氧化剂的物质的量之比是5:1,C错误;D.③还原剂是氯气,氧化剂是溴酸钾,该反应式中lmol还原剂反应则氧化剂得到电子的物质的量=2×(5-0)mol=10mol,D错误;
