硫酸亚铁铵是一种重要的化工原料,用途十分广泛.硫酸亚铁铵俗称摩尔盐,下图为制取摩尔盐过程的示意图.
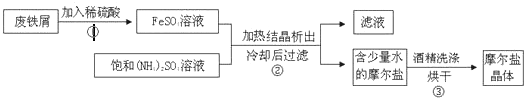
请回答下列问题:
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH______7(填“>”、“<”或“=”).
(2)步骤②中,过滤操作,需要的玻璃仪器有烧杯、玻璃棒、______能用加热结晶的方法析出说明摩尔盐的溶解度______;
(3)废铁屑的主要成分是铁,同时含有少量氧化铁.请写出①中反应的化学方程式______;______
(4)步骤②所得滤液中一定含有的溶质是______;
(5)能用酒精洗涤的原因______.
(1)碳酸钠溶液显碱性,pH>7,能除去油污;
(2)过滤操作中,需要的玻璃仪器有烧杯、玻璃棒、漏斗,能用加热结晶的方法析出说明摩尔盐的溶解度随着温度的升高而增大;
(3)废铁屑中有铁、氧化铁,铁与稀硫酸反应生成硫酸亚铁和氢气,氧化铁和稀硫酸反应生成硫酸铁和水,铁还能与硫酸铁反应生成硫酸亚铁,方程式为Fe+H2SO4═FeSO4+H2↑; 3H2SO4+Fe2O3═Fe2(SO4)3+3H2O;Fe2(SO4)3+Fe═3FeSO4;
(4)从硫酸亚铁铵的溶液中结晶析出硫酸亚铁铵,滤液中一定含有硫酸亚铁铵;
(5)由于硫酸亚铁铵不溶于酒精,所以能用酒精洗涤摩尔盐.
故答为:(1)>;(2)漏斗,溶解度随着温度的升高而增大;(3)Fe+H2SO4═FeSO4+H2↑,3H2SO4+Fe2O3═Fe2(SO4)3+3H2O;(4)硫酸亚铁铵;(5)硫酸亚铁铵不溶于酒精.
