问题
问答题
纯净的CaCO3可以用来测定盐酸的浓度.采用适当的试剂,从石灰石(主要成分是CaCO3)获得高纯度CaCO3的流程如下:
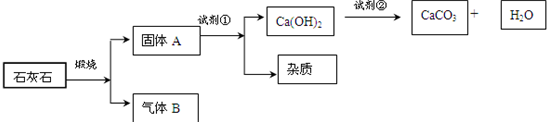
试回答:
①固体A是______;气体B是______;试剂①是______;试剂②是______.
②石灰石煅烧的化学方程式是______.
③使原料中各原子的利用率达到100%,是“绿色化学”的核心理念之一.上述流程中有的物质可以再利用,它是______.
答案
①石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,可知锻烧石灰石所得到的固体A是生石灰;气体B二氧化碳;生石灰与水反应生成氢氧化钙,故试剂①是水;氢氧化钙与水反应生成碳酸钙沉淀和水,故试剂②是二氧化碳.
②石灰石煅烧的化学方程式为:CaCO3
CaO+CO2↑. 高温 .
③石灰石的主要成分碳酸钙在高温下分解生成氧化钙和二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙和水,因此二氧化碳可以再利用;固体A需要与水反应生成氢氧化钙,而氢氧化钙与二氧化碳又生成了水,因此水也可以再利用.
故答案为:①生石灰;二氧化碳;水;二氧化碳;②CaCO3
CaO+CO2↑;③二氧化碳或水. 高温 .
