(14分)下图所示装置是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。

(1)若烧瓶中盛装Zn片,分液漏斗中盛装稀H2SO4,则:
①当制备H2、验证H2的还原性并检验H2的氧化产物,仪器连接顺序为:A→C→B
→B→D时,两次使用B装置,其中所盛的药品依次是 、
(写化学式);D装置的作用是
。
②上述实验中为了使H2产生的速率不至于过快,在不改变现有药品的条件下,可采取的方法有 、
。(要求:写出的两种方法原理不同)
(2)若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3。能产生大量NH3的原因是:
a ;b ;c 。
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→ → → (填正确序号的字母)此时在其中的一个装置中可能会出现大量红棕色气体,该装置是 (用字母表示);用化学方程式解释红棕色气体产生的原因: 、
。
(14分,方程式2分,其它每空1分)(1)① CuO、 CuSO4; 防止空气中的水进入装置,干扰H2氧化产物的检验。
②控制分液漏斗的活塞,使稀H2SO4缓慢滴下; 加水(或将烧瓶放入冰水中或用冰毛巾捂着烧瓶或加入醋酸钠固体等)(其他合理答案亦可给分)
(2)①Na2O2与水反应放热,降低NH3的溶解度(或使NH3·H2O发生分解);
Na2O2与水反应,耗水(或使水量减少),降低NH3的溶解量; Na2O2与水反应生成OH–,c(OH–)增大,抑制NH3·H2O的电离有利于NH3的逸出。
②A→D→B→E(或D)(顺序错不得分), B
4NH3+5O2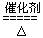 4NO+6H2O 、 2NO+O2===2NO2
4NO+6H2O 、 2NO+O2===2NO2
