(14分)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是 。
(2)“三酸”与“两碱”之间均可反应,酸过量时若用化学方程式表示有六个,若用离子方程式表示却只有两个,请写出其中能产生气体的离子方程式为 ;选取日常生活中常见物质由纯碱制烧碱的化学方程式为 。
(3)“三酸”常用于溶解金属和金属氧化物。下列块状金属不能溶于足量浓盐酸的是 。
A.Fe
B.Cu
C.Al
D.Ag(4)烧碱、纯碱均可吸收CO2,当含0.1molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况,分别是:
① ; ②Na2CO3; ③ ; ④NaHCO3
将得到的固体重新溶解于水,在溶液中加一定量硫酸,使溶液中只含一种溶质,再将溶液蒸干,得到固体的物质的量是 摩。
(14分)(1)纯碱(或Na2CO3)
(2)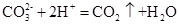 ;Ca(OH)2+Na2CO3="==" Ca CO3↓ +2NaOH
;Ca(OH)2+Na2CO3="==" Ca CO3↓ +2NaOH
(3)BD
(4)①NaOH和Na2CO3;③Na2CO3和NaHCO3 0.05
(1)从物质的分类角度看,不恰当的一种物质是纯碱,纯碱是盐,不是碱。
(2)“三酸”与“两碱”之间反应能产生气体的话,肯定有纯碱Na2CO3,写离子方程式应该是CO32-+2H+=CO2↑+H2O 由纯碱制烧碱的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓ +2NaOH
(3)不溶于盐酸的金属应该是在金属活动顺序表中排在H后面的金属,所以应选B D
(4)当含0.1molNaOH的溶液吸收一定量CO2后,可能发生两个反应
2NaOH+CO2=Na2CO3+H2O Na2CO3+H2O+CO2=2NaHCO3 当第一个反应NaOH过量时,得到的固体是①NaOH和Na2CO3;当第一个反应恰好反应完全时,得到的固体是②Na2CO3;当第一个反应完全,第二个反应不完全时,得到固体③Na2CO3和NaHCO3,当第二个反应完全时,得到固体④NaHCO3,根据题意,溶液中只含一种溶质,应该是硫酸钠,根据钠元素守恒,NaOH是0.1mol,Na2SO4应该是0.05mol.
