(12分)化学研究性学习小组拟通过实验探究“新制的还原性铁粉和过量盐酸反应生成FeCl2还是FeCl3”。请你参与探究并回答有关问题:
(1)一位同学用向反应后的溶液中滴加NaOH溶液的方法来验证溶液中含有Fe2+。①可观察到的实现现象是___________,②反应过程中发生反应的化学方程式是 。
(2)另一位同学向反应后的溶液中先滴加KSCN溶液,再向其中滴加新制氯水,溶液呈现红色,但当滴加过量新制氯水时,却发现红色褪去。为了弄清溶液红色褪去的原因,同学们查到如下资料:
Ⅰ.铁有一种化合物称为铁酸盐(含有FeO42-)。
Ⅱ.SCN-的电子式为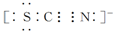
III.氯水具有很强的氧化性。
于是同学们提出两种假设:
①第一种假设是:Cl2可将Fe3+氧化为FeO42-,请写出该离子反应方程式__________。
②第二种假设是:____________,提出该假设的理论依据是___________________
(1)①产生白色沉淀,迅速变为灰绿色,最终变成红褐色
②FeCl2+2NaOH===Fe(OH)2↓+2NaCl
4Fe(OH)2+O2+2H2O===4Fe(OH)3
(2)①2Fe3++3Cl2+8H2O===2FeO+6Cl-+16H+
②SCN-被Cl2氧化 从电子式分析,SCN-中S为负二价,N为负三价,均为最低价有被氧化的可能
本题以铁元素及其化合物的知识点为基础,考查方程式书写基本功,以及提出问题,分析问题,解决问题的能力。
⑴Fe2++2OH―=Fe(OH)2↓,4Fe(OH)2+O2+2H2O===4Fe(OH)3 ①产生白色沉淀,迅速变为灰绿色,最终变成红褐色,②方程式这FeCl2+2NaOH===Fe(OH)2↓+2NaCl、
4Fe(OH)2+O2+2H2O===4Fe(OH)3;Cl2可将Fe3+氧化(2)①2Fe3++3Cl2+8H2O===2FeO+6Cl-+16H+ ②SCN-被Cl2氧化 从电子式分析,SCN-中S为负二价,N为负三价,均为最低价有被氧化的可能。
