(9分)某小组同学为探究铜跟浓硫酸的反应情况,并收集一瓶反应产生的气体,设计了如右图所示装置。实验中他们取6.4g铜片与12mL 18mol/L浓硫酸放在圆底烧瓶中加热,直到反应完毕仍发现烧瓶中有铜剩余。
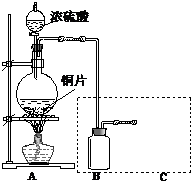
(1)为防止空气污染,请补画右图虚框中的实验装置,并注明所需要的试剂名称。
(2)写出铜跟浓硫酸反应的化学方程式:
。
(3)该小组认为铜片未完全溶解,则瓶中可能还有一定量的硫酸剩余,其原因是:
。
(4)为证明反应结束后的烧瓶中确有余酸,可选用下列药品中的 (填写字母序号):
A.铁粉
B.BaCl2溶液
C.银粉
D.Na2CO3溶液

(1)为防止空气污染,应有尾气吸收装置,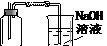
(2)写出铜跟浓硫酸反应的化学方程式:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)该小组认为铜片未完全溶解,则瓶中可能还有一定量的硫酸剩余,其原因是:
铜只与浓硫酸反应,随着反应的进行,浓硫酸变为稀硫酸,铜就不在反应,所以,溶液中肯定有稀硫酸存在。
(4)为证明反应结束后的烧瓶中确有余酸,可选用的药品是铁粉、Na2CO3溶液。加入铁粉,如果铁粉溶解并有气泡产生,证明有余酸。加入Na2CO3溶液,如果有气泡产生,证明有余酸。故选A D。
