( 16分)某兴趣小组拟利用如下图装置探究验证干燥的Cl2和潮湿的C l2有无漂白性。
l2有无漂白性。
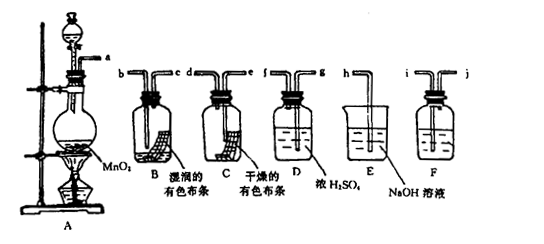
回答下列问题:
(1)A装置中的主要玻璃仪器有:导管、酒精灯、圆底烧瓶、 。
A装置中发生反应的化学方程式是 。
F装置中的试剂应为 ,作用为 。
(2)按气体从左向右流向将各装置依次连接起来(填接口标号): a 接 ,
接 , 接 , 接 , 接 。
。
(3)通入Cl2后,从集气瓶A、B中 红色布条的现象可得出的结论是
红色布条的现象可得出的结论是
;其中发生的反应的化学方程式为 。
(4)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是
。
(5)烧杯E中发生反应的化学方程式为 。
(6)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛4 mol·L-1的NaOH溶液的体积至少应为 mL。
( 16分)
16分)
(1)分液漏斗;MnO2+4HC(浓) MnCl2+2H2O+Cl2↑ ;饱和食盐水;除Cl2中的HCl
MnCl2+2H2O+Cl2↑ ;饱和食盐水;除Cl2中的HCl
(方程式2分,其余每空1分,共5分)
(2)a 接i,j接g,f接e,d接b,c接h (2分,全对才得分)
(3)干燥的Cl2没有漂白性,氯水有漂白性 (1分)
Cl2+ H2O="HCl+" HClO (2分)
(4)验证稀盐酸是否有漂白性 (1分)
(5)吸收多余的Cl2 (1分)
Cl2+2NaOH="NaCl+" NaClO+H2O (2分)
(6)100 (2分)
